2022年9月,云南省人民政府办公厅印发《云南省“十四五”中医药发展规划》,提出到2025年,中医药高质量发展体制机制进一步健全,中医药发展政策和体系更加完善,中医药服务能力明显提升,中医药事业产业发展取得积极成效,打造面向西南、辐射南亚东南亚的中药材交易中心,中医药在健康云南建设中的重要支撑作用进一步凸显。
一、我国中药材进出口情况
2021年,我国中药材进出口贸易总额达60.62亿美元,其中出口总额达40.93亿美元,同比下降了2.10%;进口总额达19.69亿美元,同比增长了42.07%,顺差21.24亿元,略低于近5年平均水平。从贸易量看,中药材进出口总量达20.52万吨,其中出口数量13.75万吨,同比下滑了4.81%;进口数量6.77万吨,同比下滑了0.59%。
东南亚国家药材资源非常丰富,是中国进口药材的主要货源地之一,有很多中国稀缺且需求量大的原药材。中国近30%数量的进口药材从东南亚进口。是全球最大的中药材消费国,常用中药材近600 种,其中约有1/10需要进口。进口中药材主要品种有乳香、没药、血竭、龙眼肉、西洋参、鹿茸等。
二、我国允许中药材进口的口岸
我国对进口药材采取指定口岸管理,药材进口边境口岸应当按需设置,且只能进口该口岸接壤及邻近国家(地区)所产的药材。增设的药材进口边境口岸,应当是已设立海关机构且具备进口药材海关监管能力的边境口岸。我国对进口中药材采取指定口岸管理,食品药品监管总局和海关总署负责对申报的药材进口边境口岸进行考核评估,考核评估合格的报国务院批准。
在全国22个边境口岸中,云南拥有德宏瑞丽、红河河口、版纳景洪、文山天保四个口岸,为进口药材数量最多的省份,进口中药材品种达29个,其中以德宏州瑞丽口岸进口量最大,2018年瑞丽口岸共进口药材7451.9吨,2019年进口中药材超过4.17万吨,占云南省对缅贸易的60%以上,占全国对缅贸易的30%左右,连续15年保持2位数高增长。
三、我国允许进境的东南亚国家药材名录
目前,我国允许进口药材的东南亚国家有菲律宾、柬埔寨、老挝、马来西亚、缅甸、泰国、新加坡、印度尼西亚和越南9个国家;其中菲律宾1种,柬埔寨1种,老挝9种,马来西亚10种,缅甸39种,泰国19种,新加坡6种,印度尼西亚19种,越南30种,多为植物源药材,动物源药材仅有地龙、蛤蚧(干制壁虎)、干海马、乌梢蛇4种。对于未在名单内的东南亚国家及药材,需完成检疫准入程序方可进口。
同时进口药材,按要求必须接受药监部门、海关部门和濒管办的三重管理。


四、海关对中药材进口如何监管?
1.检疫准入。海关总署对进境中药材实施检疫准入制度,包括产品风险分析、监管体系评估与审查、确定检疫要求、境外生产企业注册登记以及进境检疫等。
2.境外企业注册登记。海关总署根据风险分析的结果,确定需要实施境外注册登记的药材品种目录,并实施动态调整。海关总署对向中国输出需要实施境外注册登记的药材品种的境外生产企业实施注册登记,注册登记有效期为4年。
3.检疫审批。进境中药材需办理进境动植物检疫审批的,货主或者其代理人应当在签订贸易合同前,按照《进境动植物检疫审批管理办法》的规定取得《中华人民共和国进境动植物检疫许可证》。
4.现场监管。单证审核——海关接受企业申报,审核企业提交的资料是否符合法律、行政法规及海关进口货物申报管理规定的要求。
货物检查——海关根据业务系统指令对进境中药材实施口岸检查,主要包括:
(一)查询启运时间和港口、途经国家或者地区、装载清单等,核对单证是否真实有效,单证与货物的名称、数(重)量、输出国家或者地区、唛头、标记、境外生产企业名称、注册登记号等是否相符;
(二)包装是否完好,是否带有动植物性包装、铺垫材料,并符合《中华人民共和国进出境动植物检疫法》及其实施条例、进境货物木质包装检疫监督管理办法的规定;
(三)中药材有无腐败变质现象,有无携带有害生物、动物排泄物或者其他动物组织等,有无携带动物尸体、土壤及其他禁止进境物。
5.实验室检测。现场检疫中发现病虫害、病虫为害症状,或者根据相关工作程序需进行实验室检疫的,海关应当对进境中药材采样,并送实验室。
6.指定场所存放、加工。中药材在取得检疫合格证明前,应当存放在海关认可的地点,未经海关许可,任何单位和个人不得擅自调离、销售、加工。
7.检疫结果评定。进境中药材经检疫合格,海关出具“入境货物检验检疫证明”后,方可销售、使用或者在指定企业存放、加工。
8.检疫不合格处理。检疫不合格的,海关签发检疫处理通知书,由货主或其代理人在海关的监督下,作除害、退回或者销毁处理,经除害处理合格的准予进境。
9.运输工具检疫处理。装运进境中药材的运输工具和集装箱应当符合安全卫生要求。需要实施防疫消毒处理的,应当在进境口岸海关的监督下实施防疫消毒处理。未经海关许可,不得将进境中药材卸离运输工具、集装箱或者运递。
10.企业管理。境内货主或者其代理人应当建立中药材进境和销售、加工记录制度,做好相关记录并至少保存2年。同时应当配备中药材防疫安全管理人员,建立中药材防疫管理制度。
五、中药材进口许可证申请
(一)关于首次进口药材的申请与审批
1.对2020年1月1日前国家药品监督管理局已正式受理,但未完成审批的申请,仍按原有关规定审批,申请人也可以申请撤回提交的申请。
2.首次进口药材,申请人应当登录国家药品监督管理局网站网上办事大厅,通过“法人服务”项下办理首次进口药材申请,并按《办法》要求向所在地省级药品监督管理部门报送有关资料,取得《进口药材批件》。
3.各省级药品监督管理部门通过国家药品监管专网受理首次进口药材申请,并按《办法》规定实施审批。
(二)关于进口药材的备案
1.药材进口单位和口岸药品监督管理部门按照《国家药监局关于启用新版药品和药材进口备案管理系统的公告》(2019年第107号)提示,登录备案系统相应窗口在线办理进口药材备案。
2.国家药品监督管理局已对2006年、2011年发布的两批《非首次进口药材品种目录》进行了修订、合并,原有目录予以废止。凡申请进口列入目录中的药材品种,申请人无须取得《进口药材批件》,直接按照《办法》规定向口岸药品监督管理部门进行非首次进口药材备案,各口岸药品监督管理部门应按非首次进口药材进行形式审查。
一、我国中药材进出口情况
2021年,我国中药材进出口贸易总额达60.62亿美元,其中出口总额达40.93亿美元,同比下降了2.10%;进口总额达19.69亿美元,同比增长了42.07%,顺差21.24亿元,略低于近5年平均水平。从贸易量看,中药材进出口总量达20.52万吨,其中出口数量13.75万吨,同比下滑了4.81%;进口数量6.77万吨,同比下滑了0.59%。
东南亚国家药材资源非常丰富,是中国进口药材的主要货源地之一,有很多中国稀缺且需求量大的原药材。中国近30%数量的进口药材从东南亚进口。是全球最大的中药材消费国,常用中药材近600 种,其中约有1/10需要进口。进口中药材主要品种有乳香、没药、血竭、龙眼肉、西洋参、鹿茸等。
二、我国允许中药材进口的口岸
我国对进口药材采取指定口岸管理,药材进口边境口岸应当按需设置,且只能进口该口岸接壤及邻近国家(地区)所产的药材。增设的药材进口边境口岸,应当是已设立海关机构且具备进口药材海关监管能力的边境口岸。我国对进口中药材采取指定口岸管理,食品药品监管总局和海关总署负责对申报的药材进口边境口岸进行考核评估,考核评估合格的报国务院批准。
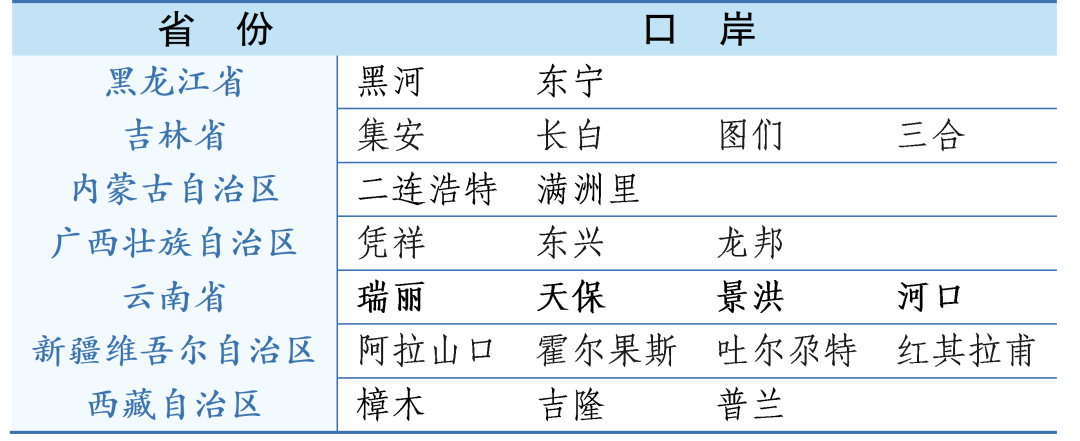
根据《进口药材管理办法》规定,药材应当从国务院批准的允许药材进口的边境口岸进口。目前,我国批准的药材进口边境口岸为22个,进口企业可根据自身需要,选择相应的(边境)口岸办理进口通关手续。
表1 我国允许药材进口的通关口岸

在全国22个边境口岸中,云南拥有德宏瑞丽、红河河口、版纳景洪、文山天保四个口岸,为进口药材数量最多的省份,进口中药材品种达29个,其中以德宏州瑞丽口岸进口量最大,2018年瑞丽口岸共进口药材7451.9吨,2019年进口中药材超过4.17万吨,占云南省对缅贸易的60%以上,占全国对缅贸易的30%左右,连续15年保持2位数高增长。
三、我国允许进境的东南亚国家药材名录
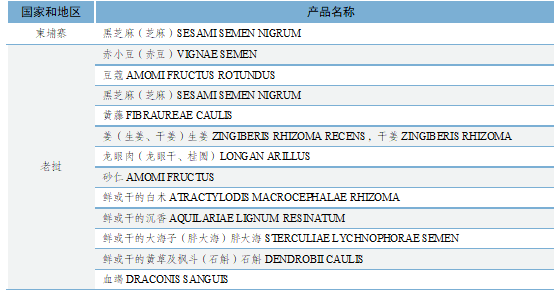
目前,我国允许进口药材的东南亚国家有菲律宾、柬埔寨、老挝、马来西亚、缅甸、泰国、新加坡、印度尼西亚和越南9个国家;其中菲律宾1种,柬埔寨1种,老挝9种,马来西亚10种,缅甸39种,泰国19种,新加坡6种,印度尼西亚19种,越南30种,多为植物源药材,动物源药材仅有地龙、蛤蚧(干制壁虎)、干海马、乌梢蛇4种。对于未在名单内的东南亚国家及药材,需完成检疫准入程序方可进口。
同时进口药材,按要求必须接受药监部门、海关部门和濒管办的三重管理。
表2 获得我国检疫准入的东南亚国家植物源性中药材名录




表3 获得我国检疫准入的东南亚国家动物源性中药材名录

四、海关对中药材进口如何监管?
1.检疫准入。海关总署对进境中药材实施检疫准入制度,包括产品风险分析、监管体系评估与审查、确定检疫要求、境外生产企业注册登记以及进境检疫等。
2.境外企业注册登记。海关总署根据风险分析的结果,确定需要实施境外注册登记的药材品种目录,并实施动态调整。海关总署对向中国输出需要实施境外注册登记的药材品种的境外生产企业实施注册登记,注册登记有效期为4年。
3.检疫审批。进境中药材需办理进境动植物检疫审批的,货主或者其代理人应当在签订贸易合同前,按照《进境动植物检疫审批管理办法》的规定取得《中华人民共和国进境动植物检疫许可证》。
4.现场监管。单证审核——海关接受企业申报,审核企业提交的资料是否符合法律、行政法规及海关进口货物申报管理规定的要求。
货物检查——海关根据业务系统指令对进境中药材实施口岸检查,主要包括:
(一)查询启运时间和港口、途经国家或者地区、装载清单等,核对单证是否真实有效,单证与货物的名称、数(重)量、输出国家或者地区、唛头、标记、境外生产企业名称、注册登记号等是否相符;
(二)包装是否完好,是否带有动植物性包装、铺垫材料,并符合《中华人民共和国进出境动植物检疫法》及其实施条例、进境货物木质包装检疫监督管理办法的规定;
(三)中药材有无腐败变质现象,有无携带有害生物、动物排泄物或者其他动物组织等,有无携带动物尸体、土壤及其他禁止进境物。
5.实验室检测。现场检疫中发现病虫害、病虫为害症状,或者根据相关工作程序需进行实验室检疫的,海关应当对进境中药材采样,并送实验室。
6.指定场所存放、加工。中药材在取得检疫合格证明前,应当存放在海关认可的地点,未经海关许可,任何单位和个人不得擅自调离、销售、加工。
7.检疫结果评定。进境中药材经检疫合格,海关出具“入境货物检验检疫证明”后,方可销售、使用或者在指定企业存放、加工。
8.检疫不合格处理。检疫不合格的,海关签发检疫处理通知书,由货主或其代理人在海关的监督下,作除害、退回或者销毁处理,经除害处理合格的准予进境。
9.运输工具检疫处理。装运进境中药材的运输工具和集装箱应当符合安全卫生要求。需要实施防疫消毒处理的,应当在进境口岸海关的监督下实施防疫消毒处理。未经海关许可,不得将进境中药材卸离运输工具、集装箱或者运递。
10.企业管理。境内货主或者其代理人应当建立中药材进境和销售、加工记录制度,做好相关记录并至少保存2年。同时应当配备中药材防疫安全管理人员,建立中药材防疫管理制度。
五、中药材进口许可证申请
(一)关于首次进口药材的申请与审批
1.对2020年1月1日前国家药品监督管理局已正式受理,但未完成审批的申请,仍按原有关规定审批,申请人也可以申请撤回提交的申请。
2.首次进口药材,申请人应当登录国家药品监督管理局网站网上办事大厅,通过“法人服务”项下办理首次进口药材申请,并按《办法》要求向所在地省级药品监督管理部门报送有关资料,取得《进口药材批件》。
3.各省级药品监督管理部门通过国家药品监管专网受理首次进口药材申请,并按《办法》规定实施审批。
(二)关于进口药材的备案
1.药材进口单位和口岸药品监督管理部门按照《国家药监局关于启用新版药品和药材进口备案管理系统的公告》(2019年第107号)提示,登录备案系统相应窗口在线办理进口药材备案。
2.国家药品监督管理局已对2006年、2011年发布的两批《非首次进口药材品种目录》进行了修订、合并,原有目录予以废止。凡申请进口列入目录中的药材品种,申请人无须取得《进口药材批件》,直接按照《办法》规定向口岸药品监督管理部门进行非首次进口药材备案,各口岸药品监督管理部门应按非首次进口药材进行形式审查。


